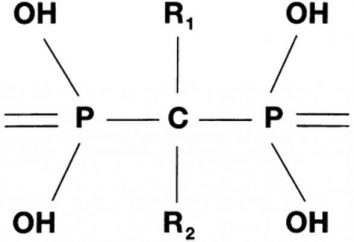
idrocarburi insaturi: alcheni, proprietà chimiche e applicazione
Alcheni – idrocarburi insaturi cui molecole tra due atomi di carbonio, un doppio legame. Essi sono spesso chiamati serie idrocarburi etilene, perché è un semplice etilene rappresentante NC2 = CH2. olefine Talvolta questi idrocarburi vengono definiti come alcheni gassosi reagiscono con cloro o bromo per formare composti oleosi che non sono solubili in acqua. La parola "alcheni" nomenclatura IUPAC deriva dalla parola "alcani", dove suffisso -un è sostituito dal -ene suffisso, che indica la presenza nella molecola della sostanza del doppio legame.
idrocarburi insaturi – alcheni: struttura
Tutti alcheni considerati derivati di etilene o etene – C2H4.
La molecola di etilene contiene due atomi di carbonio e quattro atomi di idrogeno, atomi di carbonio insaturi. Ciascuno di carbonio insaturo atomo ibridizza es uno e due pi-orbitali, e rimane una pi orbitali in "forma pura", che fornisce la distanza massima degli orbitali elettronici ibridati. i loro assi formano 120 °. Ciò crea le condizioni ottimali per la sovrapposizione di orbitali elettronici. Tre tali orbitali di atomi di carbonio per formare tre legami sigma (due C-H, C-C a). Di conseguenza, la molecola di etilene ha cinque legami sigma che sono localizzate nello stesso piano, formando fra loro un angolo di 120 °. P-elettroni che rimangono nel "puro" formano un altro legame tra due atomi di carbonio. Descritto struttura elettronica di molecole di etilene tipici di alcheni. idrocarburi insaturi sono da considerarsi come derivati di etilene.
Per alchene caratterizzato da 2 tipi di isomeria – geometriche e strutturali.
isomeri strutturali di alcheni inizia con butene C4H8. Distinguere e sue varianti – catena isomeria (o scheletro di carbonio) e isomeri collocamento del doppio legame in un tale circuito.
isomeria geometrica a causa del posizionamento irregolare dei sostituenti idrogeno nella molecola di etilene rispetto al piano del doppio legame. idrocarburi insaturi sono cis e trans isomeri.
Alcheni in stato libero è molto raro in natura. Essi sono stati sintetizzati con processi industriali e di laboratorio.
proprietà chimiche di idrocarburi: alcheni
Essi sono causati da un doppio legame tra due atomi di carbonio nella molecola di un alchene.
La reazione di idrogenazione
Alcheni reagiscono prontamente attaccamento di idrogeno. Essa si verifica in presenza di catalizzatori o con riscaldamento:
CH2 = CH2 = H2 H3C CH3
unendo alogenuri
La reazione procede per la regola Markovnikov, cioè facendo reagire un alogenuro di idrogeno con molecole asimmetriche alcheni idrogeno viene aggiunto al posto della localizzazione del doppio legame preferibilmente all'atomo di carbonio accanto al quale vi sono più atomi di idrogeno, un atomo di alogeno – all'atomo di carbonio accanto a cui meno atomi di idrogeno o completamente non esistono:
CH3-CH = CH2 + HC1-CH3-CH3-CHC1.
L'uso di idrocarburi
Ethene – gas scioglie bene in alcool e scarsamente solubile in acqua, esplosiva.
Essi sono ricchi di gas di cracking (fino al 20% del peso totale) e gas di cokeria (circa il 5%). Nei metodi di laboratorio di disidratazione di etilene preparato deidrogenazione di etano ed etanolo. Applicato per ottenere etilene alcool etilico, cloruro di vinile, etilbenzile, polietilene, agenti antigelo (sostanze che riducono il punto di congelamento dell'acqua nei motori) e altre sostanze organiche. In medicina umana e veterinaria, l'etilene è utilizzato come una formulazione di droga in coltura – per accelerare la maturazione dei frutti (pomodori, limoni, e simili).
Propilene è ottenuto insieme con etilene nella pirolisi e di cracking di vari tipi di rifornimento di petrolio. Propilene – un componente del carburante. E 'utilizzato come materia prima per il polipropilene, isopropylbenzyl, alcool isopropilico. Con isopropanolo, acetone, con isopropylbenzyl – acetone e fenolo. Propilene è utilizzato come farmaco narcotico per sintetizzare acrilonitrile, cumene, butanolo, ecc