Le proprietà chimiche di alchini. La struttura, preparazione, applicazione
Alcani, alcheni, alchini – è sostanze chimiche organiche. Tutti sono costruiti di tali elementi chimici come il carbonio e l'idrogeno. Alcani, alcheni, alchini – sono composti chimici, che appartengono al gruppo idrocarburico.
In questo articolo vedremo alchini.
Di cosa si tratta?
Queste sostanze sono anche chiamati idrocarburi acetilene. La struttura della alchino prevede la presenza nelle molecole di idrogeno e carbonio atomi. General formula acetilenici idrocarburi quali: C n H 2n-2. Il più semplice semplice alchino – ethyne (acetilene). E qui ha una formula chimica – C 2 H 2. si riferisce anche ad alchini propyne della formula C 3 N 4. Inoltre, per acetilenici idrocarburi possono includere butino (C 4 H 6), Pentin (C 5 H 8) esino (C 6 H 10) heptyn (C 7 H 12), octyne (C 8 H 14), nonyne ( C 9 H 16) decyne (C 10 H 18), e così via. d. Tutti i tipi di alchini presentano caratteristiche simili. Diamo loro Esaminiamo in dettaglio. 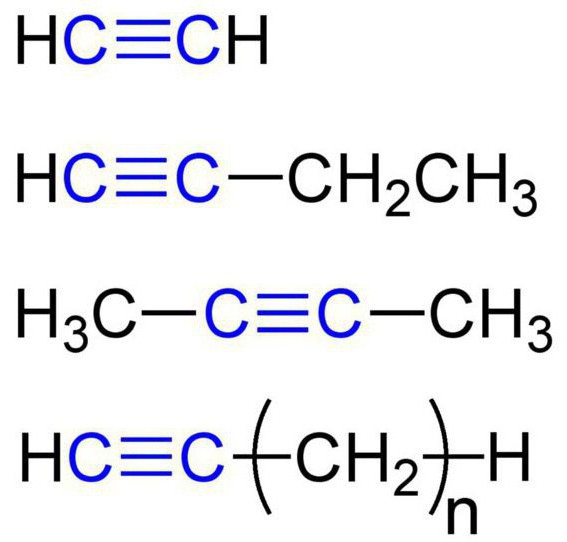
Le proprietà fisiche di alchini
Le caratteristiche fisiche degli idrocarburi acetilene ricordano alcheni.
In condizioni normali, alchini, cui molecola contiene da due a quattro atomi di carbonio, avere uno stato aggregato gassoso. Quelle molecole di cui è da cinque a 16 atomi di carbonio, in normali condizioni di liquido. Quelle delle molecole di cui 17 o più atomi di un elemento chimico, – solidi.
Alchini fondono e bollire a temperatura superiore ai alcani e alcheni.
Solubilità in acqua è insignificante, ma leggermente superiore a quello di alcheni e alcani.
Solubilità in solventi organici è elevato.
L'alchino più usato – acetilene – ha tali proprietà fisiche:
- Essa non ha colore;
- inodore;
- in condizioni normali, è in uno stato gassoso di aggregazione;
- Ha una densità inferiore a quella dell'aria;
- punto di ebollizione – meno 83,6 gradi Celsius;
Le proprietà chimiche di alchini
In queste sostanze, gli atomi sono legati triplo legame, che spiega le loro proprietà fondamentali. Alchini reagiscono questo tipo:
- idrogenazione;
- gidrogalogenirovanie;
- alogenazione;
- idratazione;
- bruciando.
Diamo loro prendere in ordine. 
idrogenazione
Le proprietà chimiche di alchini permettono loro di impegnarsi in questo tipo di reazione. Questo tipo di interazioni chimiche, in cui la molecola sostanza si attacca ad atomi di idrogeno aggiuntivi. Ecco un esempio di una tale reazione chimica nel caso di propyne:
2H 2 + C 3 H 4 = C 3 H 8
Questa reazione avviene in due fasi. Nella prima molecola propyne allega due atomi di idrogeno, e la seconda – la stessa quantità.
alogenazione
Questa è un'altra reazione, che è parte delle proprietà chimiche del alchini. Il suo risultato molecola di idrocarburo acetilenico attribuisce atomi di alogeno. Questi ultimi comprendono elementi come cloro, bromo, iodio, ecc
Ecco un esempio di una tale reazione in caso di etinil:
C 2 H 2 + 2SІ 2 = C 2 H 2 s² 4
Lo stesso processo è possibile anche con altri idrocarburi acetilenici.
Gidrogalogenirovanie
E 'anche uno dei principali reazioni, che fa parte delle proprietà chimiche di alchini. Esso consiste nel fatto che la sostanza viene fatto reagire con composti come NSІ, ni, HBr, e altri. Questa reazione chimica avviene in due fasi. Diamo un'occhiata alla reazione di questo tipo sull'esempio di etinilestradiolo:
C 2 H 2 + NSІ = C 2 H 3 s²
C 2 H 2 + s² NSІ = C 2 H 4 s² 2 
idratazione
Questa è una reazione chimica che è in contatto con l'acqua. Essa si verifica anche in due fasi. Diamo un'occhiata a che sull'esempio di etinilestradiolo:
H 2 O + C 2 H 2 = C 2 H 3 OH
Una sostanza che si forma dopo la reazione di primo stadio chiamato alcol vinilico.
A causa del fatto che, secondo la regola Eltekova OH gruppo funzionale non può essere adiacente al doppio legame, riarrangiamento di atomi, in conseguenza della quale l'alcol vinilico è formato acetaldeide.
Il processo di reazione di idratazione chiamato anche alchino Kucherova. 
ardente
Questo processo di interazione alchini con ossigeno ad alta temperatura. Considerate le sostanze di questo gruppo che brucia con acetilene, ad esempio:
2C 2 H 2 + 2O 2 = 2H 2 O + CO 2 + 3C
Quando un eccesso di ossigeno, acetilene, e altri alchini bruciano senza la formazione di carbonio. Così ripartiti soltanto monossido di carbonio e acqua. Ecco l'equazione di questa reazione con per esempio propyne:
4O 2 + C 3 H 4 = 2H 2 O + 3SO 2
Brucia altri idrocarburi acetilenici si verifica anche in modo simile. Di conseguenza, l'acqua viene rilasciata e anidride carbonica.
altre reazioni
Anche acetileni sono in grado di reagire con i sali di metalli come argento, rame e calcio. Così v'è una sostituzione di atomi di metallo idrogeno. Considerate questo esempio in vista della reazione con nitrato di acetilene e argento:
C 2 H 2 + 2AgNO3 = Ag 2 C 2 + 2NH 4 NO 3 + 2H 2 O
Un altro processo interessante che coinvolge alchini – reazione Zelinsky. Questa formazione di benzene da acetilene quando è riscaldato a 600 ° C in presenza di carbone attivo. L'equazione per questa reazione può essere espresso come segue:
3C 2 H 2 = C 6 H 6
polimerizzazione di alchini possibile – il processo di associazione di diverse molecole della sostanza in un polimero. 
reception
reazione alchino che abbiamo discusso in precedenza, sono preparati in laboratorio in diversi modi.
Il primo – un deidroalogenazione. Sembra equazione di reazione in tal modo:
C 2 H 4 Br 2 + 2KOH = C 2 H 2 + 2H 2 O + 2KBr
Per eseguire questo processo è di riscaldare i reagenti, e aggiungere etanolo come catalizzatore.
Inoltre v'è la possibilità di alchini da composti inorganici. Ecco un esempio:
CaC 2 + H 2 O = C 2 H 2 + 2CA (OH) 2
Il prossimo metodo di produzione alkyne – deidrogenazione. Ecco un esempio di una tale reazione:
= 3H 2 CH 4 + 2 C 2 H 2
Con questo tipo di reazione può essere ottenuta non solo ethyne, ma altri idrocarburi acetilenici.

L'uso di alchino
Il più ampiamente utilizzato nel settore è stata la più semplice alkyne – ethyne. È ampiamente usato nell'industria chimica.
- Necessaria acetilene o altri alchini per produrre uno altri composti organici come chetoni, aldeidi, e altri solventi.
- Anche da alchini possono essere ottenuti sostanze utilizzate nella fabbricazione di gomme, cloruro di polivinile e altri.
- Da propyne può essere ottenuto come acetone risultato RAKTs Kucherova.
- Inoltre, acetilene viene utilizzato nella preparazione di sostanze chimiche come acido acetico, idrocarburi aromatici, alcool etilico.
- Ulteriori acetilene è utilizzato come combustibile con un elevato calore di combustione.
- Anche reazione di combustione etinil è utilizzato per la saldatura dei metalli.
- Inoltre, utilizzando un acetilene, può essere preparato Carbonio tecnico.
- Inoltre, questa sostanza è utilizzata in apparecchi stand-alone.
- Acetilene e altri idrocarburi numero di questo gruppo sono utilizzati come propellenti grazie al suo elevato calore di combustione.
In questa applicazione alchini termina. 
conclusione
Come la parte finale della tabella è un riepilogo delle proprietà degli idrocarburi acetilene e la loro preparazione.
| Nome reazioni | spiegazioni | esempio equazione |
| alogenazione | reazione di addizione di una molecola degli atomi di alogeno idrocarburi acetilenici (bromo, iodio, cloro, ecc). | C 4 H 6 + 2I 2 = C 4 H 6 di I 2 |
| idrogenazione | reazione di addizione di un alchino atomi di idrogeno della molecola. Esso avviene in due fasi. |
C 3 H 4 + H 2 = C 3 H 6 C 3 H 6 + H 2 = C 3 H 8 |
| Gidrogalogenirovanie | reazione di addizione dell'acetilene gidrogalogenov idrocarburi molecola (ni, NSІ, HBr). Esso avviene in due fasi. |
C 2 H 2 + ni = C 2 H 3 di I C 2 H 3 + ni di I = C 2 H 4 I 2 |
| idratazione | Le reazioni, che si basa sulla interazione con l'acqua. Esso avviene in due fasi. |
C 2 H 2 + H 2 O = C 2 H 3 OH C 2 H 3 OH = CH 3 CHO |
| La completa ossidazione (combustione) | Atsetilenovgo reagire idrocarburo con ossigeno a temperatura elevata. Questo produce monossido di carbonio e acqua. |
2C 2 H 5 + 5O 2 = 2H 2 O + 4CO 2 2C 2 H 2 + 2O 2 = H 2 O + CO 2 + 3C |
| Reazioni con sali metallici | Esso consiste nel fatto che gli atomi di metallo sono sostituiti con atomi nelle molecole di idrogeno idrocarburi acetilenici. |
C 2 H 2 + AgNO3 = C 2 Ag 2 + 2NH 4 NO 3 + 2H 2 O |
Ricevi alchini possono essere in laboratorio utilizzando tre metodi:
- composti inorganici;
- per deidrogenazione di composti organici;
- Metodo deidroalogenazione di sostanze organiche.
Così abbiamo guardato tutte le caratteristiche fisiche e chimiche del alkyne, i loro metodi di preparazione, applicazioni nel settore.














