Al fine di stabilire la composizione qualitativa di molti alimenti utilizzati reazione ksantoproteinovaya alla proteina. La presenza di aminoacidi aromatici nel mix cambierà in un colore campione di test positivo.
Che cosa è la proteina
Si chiama anche una proteina, che è un materiale da costruzione per il corpo vivente. Le proteine mantengono dimensione del muscolo, ripristinare le strutture dei tessuti feriti e morti di vari organi, che si tratti di capelli, pelle e legamenti. Con la loro partecipazione, produce globuli rossi, è governato dal normale funzionamento di molti ormoni e cellule del sistema immunitario. 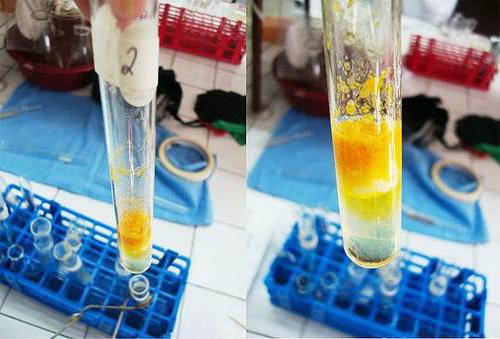
Questa è una molecola complessa che è un polipeptide avente una massa maggiore di 6 ~ 10 3 dalton. struttura proteica formando residui amminoacidici in un gran numero di legame peptidico accoppiato.
La struttura delle proteine
La caratteristica distintiva di queste sostanze rispetto ai peptidi a basso peso molecolare è che hanno sviluppato una struttura spaziale tridimensionale, effetti con vari gradi di attrazione supportati. Proteine possiedono quattro struttura. Per ognuno di loro ha le proprie caratteristiche.
Come base principale organizzazione delle molecole derivate sequenza di amminoacidi, struttura che riconosce reazione ksantoproteinovaya alla proteina. Questa struttura è un periodicamente ripetuto legame peptidico -HN-CH-CO-, un selettivo radicali parte sono le catene laterali di amminoacidi. Essi definiscono altre proprietà della sostanza nel suo complesso.
La struttura proteica primario è considerato abbastanza forte, questo è dovuto alla presenza di forti interazioni covalenti in legami peptidici. La formazione di livelli successivi avviene seconda delle attributi impostati nella fase iniziale.
La formazione della struttura secondaria è possibile grazie alla torsione della sequenza amminoacidica in una spirale, in cui sono stabiliti legami idrogeno tra le spire.
organizzazione terzo livello di molecole formato applicando uno di una spirale sugli altri frammenti con il verificarsi di tutte le possibili connessioni tra di loro, con idrogeno, disolfuro, covalente o composto ionico. Il risultato è l'associazione in forma di globuli. 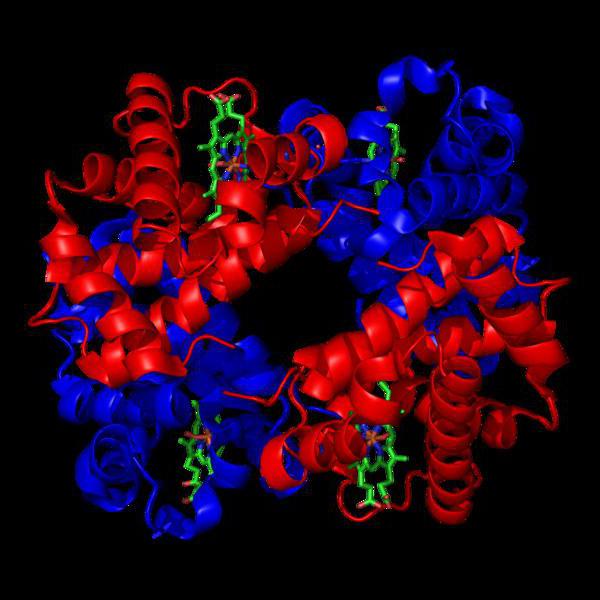
La disposizione spaziale delle strutture terziarie con la formazione di legami chimici tra loro porta alla formazione della forma finale della molecola o livelli quaternari.
aminoacidi
Essi causano le proprietà chimiche delle proteine. Ci sono circa 20 importanti aminoacidi che compongono i polipeptidi in una sequenza diversa. Questo acido amminocarbossilico rara anche viene indicato nella forma idrossiprolina e idrossilisina derivato peptidico di base.
Come segno di reazione proteine riconoscimento ksantoproteinovaya, la presenza di alcuni aminoacidi fornisce il cambiamento di colore dei reagenti, suggerendo la presenza di strutture specifiche nella loro composizione.
Come si è scoperto, sono acidi carbossilici che si sono verificati sostituzione di un atomo di idrogeno sul gruppo amminico.
Una struttura esempio della molecola può servire una formula strutturale glicina (HNH- HCH- COOH) come amminoacido più semplice. 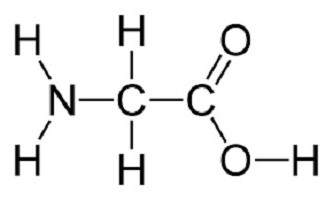
In questo caso uno degli idrogeni CH 2 – può essere sostituito da un carbonio più radicale comprendente un anello benzenico, ammino, sulfo, carbossi.
Che cosa significa la reazione ksantoproteinovaya
Per l'analisi qualitativa di proteine usando varie tecniche. Questi includono le reazioni:
- biureto con la comparsa di colore viola;
- ninidrina per formare una soluzione blu-violetto;
- formaldeide con la costituzione di un colore rosso;
- Nogier per far precipitare il colore grigio-nero.
Nello svolgere ogni metodo ha dimostrato la presenza di proteine e la presenza di alcuni gruppi funzionali nella molecola.
Ci ksantoproteinovaya reazione alla proteina. E 'chiamata anche la ripartizione Mulder. Si riferisce alle reazioni di colore per proteine, in cui ci sono gli amminoacidi aromatici ed eterociclici.
Una caratteristica di un tale processo campione è nitrazione acido nitrico residui di amminoacido ciclico in particolare l'adesione del gruppo nitro all'anello benzenico.
Il risultato di questo processo è la formazione di composti nitro, che precipita. Questa è la reazione di base funzione ksantoproteinovaya.
Che determinato l'aminoacido
Non tutte acido amminocarbossilico può essere rilevata utilizzando un campione simile. La caratteristica principale della reazione di rilevazione delle proteine ksantoproteinovaya – la presenza del ring benzene o eterociclico negli aminoacidi molecola.
Poiché la proteina è isolata da acidi amminocarbossilici due aromatici, in cui v'è un gruppo fenile (per fenilalanina), e un idrossifenil radicale (in tirosina). 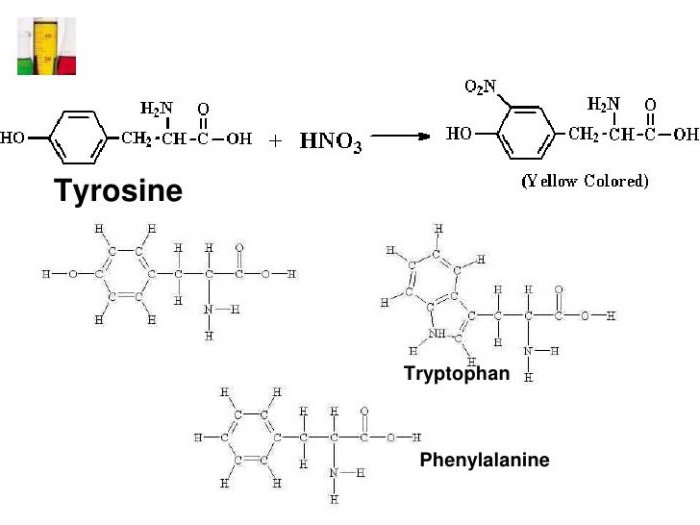
Con reazione ksantoproteinovaya è determinato eterociclico triptofano, indolo avente un nucleo aromatico. La presenza dei suddetti composti della proteina dà la caratteristica cambiamento di colore dell'ambiente di prova.
Quale uso reagenti
Per condurre la reazione ksantoproteinovaya necessario preparare una soluzione all'1% di proteine dell'uovo, o vegetale.
Solitamente utilizzato uovo, che è diviso per ulteriore separazione della proteina dal tuorlo. Per una soluzione all'1% di proteine è stato diluito in una quantità dieci volte di acqua purificata. Dopo la dissoluzione del liquido proteina risultante deve essere filtrata attraverso diversi strati di garza. Questa soluzione deve essere conservato in un luogo fresco.
E 'possibile effettuare la reazione con una proteina vegetale. Per preparare la soluzione viene utilizzata farina di grano in una quantità di 0,04 kg. 0,16 l di acqua purificata. Gli ingredienti sono stati miscelati in un pallone che è legato per 24 ore in un luogo fresco ad una temperatura di circa + 1 ° C Alla fine della giornata la soluzione è stata agitata, seguita da filtrazione della stessa prima con cotone idrofilo e poi – un foglio piegato filtro. Il liquido risultante è stato conservato in un luogo fresco. Questa soluzione è principalmente presente nella frazione albumina.
Per l'esecuzione del ksantoproteinovaya reazione come il principale reagente utilizzato conc acido nitrico. Ulteriori reagenti è una soluzione di idrossido di sodio al 10% o ammoniaca, soluzione di gelatina e fenolo non concentrata.
La metodologia del
In una provetta pulita è fatto 1% uova -esimo soluzione proteica o farina in una quantità di 2 ml. A questo si aggiunge circa 9 gocce di acido nitrico concentrato flocculazione fermato. La miscela risultante è stata riscaldata, risultante precipitato giallo scompare gradualmente e il suo colore passa in soluzione. 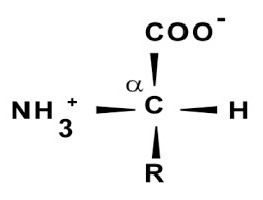
Quando il liquido si raffredda nel tubo lungo la parete aggiunto circa 9 gocce di idrossido di sodio, concentrati, che è in eccesso per il processo. Il mezzo di reazione diventa alcalina. Contenuto diventa di colore arancione in provetta.
Caratteristiche di
Poiché ksantoproteinovaya chiamato reazione qualitativa all'acido nitrico dall'azione delle proteine, il campione viene eseguita sotto incluso cappa. Osservare tutte le precauzioni di sicurezza quando si lavora con sostanze caustiche concentrate.
Il rilascio del contenuto del tubo può verificarsi durante il processo di riscaldamento che deve essere considerato quando fissaggio in un supporto e selezionando l'inclinazione.
Composizione di acido nitrico concentrato e soda caustica dovrebbe solo con una pipetta di vetro e le pere in gomma pipetta proibiti da bocca.
reazione relativa con fenolo
Per chiarezza, il processo e la conferma della presenza dei gruppi fenile viene condotta con un simile hydroxybenzene campione.
Il tubo realizzando 2 ml di fenolo diluito, poi gradualmente lungo la parete, è stato aggiunto 2 ml di acido nitrico concentrato. La soluzione è stata sottoposta a riscaldamento, cui diventa giallo. Questa reazione è la qualità della presenza dell'anello benzenico. 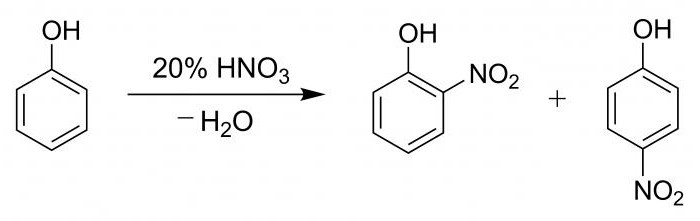
Processo idrossibenzene nitrato con acido nitrico, seguito dalla formazione di una miscela di p-nitrofenolo e o-nitrofenolo in una percentuale del 15 a 35.
test di confronto con la gelatina
Per dimostrare che la reazione ksantoproteinovaya alla proteina rivela un aminoacido con struttura aromatica, utilizzare proteine che non hanno un gruppo fenolico.
In una provetta pulita è fatto 1% soluzione di gelatina in una quantità di 2 ml. A questo si aggiunge circa 9 gocce di acido nitrico concentrato. La miscela risultante viene riscaldata. La soluzione non è stata colorata in giallo, che dimostra l'assenza di amminoacidi con una struttura aromatica. A volte c'è un leggero ingiallimento dell'ambiente dovuto alla presenza di impurità proteiche.
equazioni chimiche
Nei due step di reazione scorre ksantoproteinovaya proteine. Formula primo processo di nitrazione fase descrive molecole di amminoacidi con acido nitrico concentrato.
Un esempio è il fissaggio del gruppo nitro alla tirosina per formare nitrotirosina e dinitrotirozina. Nel primo caso all'anello benzenico è attaccato uno NO 2 -radical, e il secondo composto ha due atomi di idrogeno sono sostituiti da NO 2. Formula ksantoproteinovaya reazione chimica tirosina rappresentata mediante reazione con acido nitrico per formare molecola nitrotirosina.
processo di nitrazione è accompagnato da transizione colorazione incolore in tono giallo. Nell'effettuare tale reazione con proteine contenenti l'aminoacido residui fenilalanina o triptofano, e il colore delle modifiche soluzione.
Il secondo passo è il prodotto di reazione di nitrazione di molecole di tirosina, in particolare nitrotirosina, con ammonio o idrossido di sodio. Il risultato è un sale di sodio o di ammonio in cui il colore giallo-arancio. Tale reazione è legato alla possibilità di molecole nitrotirosina muovono nella forma quinoid. Successivamente sale formato da essa acido nitronic, che ha un sistema chinone di doppi legami coniugati. 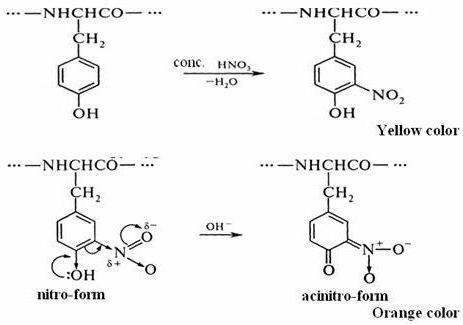
così finisce reazione ksantoproteinovaya alle proteine. L'equazione sopra presentata secondo passo.
risultati
Durante l'analisi di fluidi contenuti nei tre tubi, la soluzione di riferimento viene diluita con fenolo. Sostanze aventi un anello benzenico danno reazione qualitativa con acido nitrico. Di conseguenza, cambia il colore della soluzione.
Come è noto, gelatina comprende una forma idrolizzato di collagene. La proteina non contiene la struttura aromatica degli amminoacidi. Nessun cambiamento di colore del mezzo per reazione con un acido.
Nella terza provetta c'è una reazione positiva per proteine ksantoproteinovaya. Conclusione può essere disegnato come segue: tutte le proteine con struttura aromatica, sia esso un gruppo fenile o un anello indolo, dato il cambiamento di colore della soluzione. Ciò è dovuto alla formazione di composti nitro con un colore giallo.
Eseguire una reazione di colore dimostra la presenza di varie strutture chimiche di amminoacidi e proteine. ESEMPIO gelatina dimostra che la composizione comprende acido amminocarbossilico non avente un gruppo fenile o una struttura ciclica.
Con ksantoproteinovaya reazione si spiega con ingiallimento della pelle quando applicato ad essa un forte acido nitrico. Lo stesso colore diventerà latte schiumoso nel corso della sua analisi simili.
Nella pratica clinica di laboratorio questo campione di colore non viene utilizzato per la rilevazione di proteine nelle urine. Ciò è dovuto al colore giallo delle urine per sé.
reazione Ksantoproteinovaya diventato sempre più utilizzata per la quantificazione di aminoacidi come triptofano e tirosina, come parte di varie proteine.