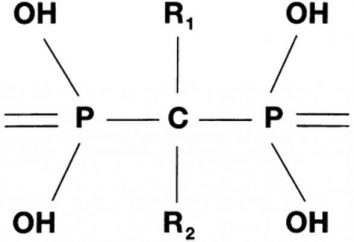
Le proprietà chimiche e fisiche di ferro
Ferro – un elemento chimico noto. Si riferisce alla media del metallo reattivo. Proprietà e applicazioni di ferro saranno discussi in questo articolo.
La prevalenza in natura
C'è piuttosto una grande quantità di minerali, tra cui Ferrum. Prima di tutto, si tratta di magnetite. Ha settantadue per cento è costituito da ferro. La sua formula chimica – Fe 3 O 4. Questo minerale noto anche come la magnetite. Ha un colore grigio chiaro, a volte con un grigio scuro al nero con una lucentezza metallica. Il suo più grande deposito si trova negli Urali nella CSI.

Successivo minerale con un alto contenuto di ferro – ematite – che comprende il settanta per cento di questo elemento. La sua formula chimica – Fe 2 O 3. E 'chiamata anche ematite. Ha un colore dal rosso-bruno al rosso-grigio. La più grande miniera della CSI è in Kryvyi Rih.
Il terzo contenuto minerale FERRUM – limonite. Qui ferro shestdesyat per cento del peso totale. Questo cristallino, cioè nella sua molecola acqua tessuto reticolo cristallino, la sua formula chimica – Fe 2 O 3 • H 2 O. Come suggerisce il nome, questo minerale ha un colore giallo-bruno, talvolta marrone. È uno dei principali componenti di ocra naturale ed è usato come pigmento. E 'chiamata anche limonite. Il più grande luogo di ritrovamento – Crimea, gli Urali.
La siderite, il cosiddetto siderite, quarantotto per cento di Ferrum. La sua formula chimica – FeCO 3. La sua struttura non è omogenea e consiste in un colore diverso sono collegati tra cristalli: grigio, verde pallido, grigio-giallo, giallo-marrone, e altri.
Quest'ultimo è spesso un minerale naturale con alto contenuto FERRUM – pirite. Ha una formula chimica FeS 2. Ferro in essa è quarantasei per cento del peso totale. A causa gli atomi di zolfo del minerale ha un colore giallo oro.
Molti dei minerali esaminati utilizzati per la produzione di ferro puro. Inoltre, l'ematite è utilizzata per la fabbricazione di gioielli da pietre naturali. inclusioni di pirite possono essere presenti in gioielleria da lapislazzuli. Inoltre, la natura del ferro trovato nella composizione degli organismi viventi – è una delle componenti più importanti della cellula. Questo oligoelemento deve entrare nel corpo umano in quantità sufficiente. Proprietà medicinali di ferro, è dovuto al fatto che questo elemento chimico è la base della emoglobina. Pertanto, l'uso di Ferrum è buono per la condizione del sangue, e di conseguenza l'intero organismo.
Hardware: proprietà fisiche e chimiche
Prendere in considerazione l'ordine di queste due grandi sezioni. Proprietà fisiche di ferro – è il suo aspetto, la densità, punto di fusione, ecc Questo è, tutte le caratteristiche distintive delle sostanze che sono associati con la fisica … proprietà chimiche del ferro – è la sua capacità di reagire con altri composti. Cominciamo con la prima.
Le proprietà fisiche di ferro
Nella sua forma pura in condizioni normali è un solido. Ha un colore grigio-argento e una lucentezza metallica pronunciato. Proprietà meccaniche comprendono livello di ferro durezza della scala Mohs. È uguale a quattro (medio). Ferro ha buona conduttività elettrica e la conducibilità termica. Quest'ultima caratteristica può essere sentito toccando l'oggetto di ferro in una stanza fredda. Dal momento che questo materiale conduce il calore in fretta, lui in un breve periodo di tempo prende una grande parte della vostra pelle, in modo da sentire freddo.  Toccare, ad esempio, alla struttura, va notato che la sua conducibilità termica è molto più basso. Le proprietà fisiche di ferro – che la sua temperatura di fusione e di ebollizione. Il primo è 1539 gradi Celsius, e la seconda – 2860 gradi Celsius. Si può concludere che le proprietà caratteristiche di ferro – buona plasticità e fluidità. Ma non è tutto.
Toccare, ad esempio, alla struttura, va notato che la sua conducibilità termica è molto più basso. Le proprietà fisiche di ferro – che la sua temperatura di fusione e di ebollizione. Il primo è 1539 gradi Celsius, e la seconda – 2860 gradi Celsius. Si può concludere che le proprietà caratteristiche di ferro – buona plasticità e fluidità. Ma non è tutto.
Anche nelle proprietà fisiche del ferro e parte di esso è ferromagnetico. Di cosa si tratta? Ferro, le proprietà magnetiche di cui possiamo vedere in esempi pratici tutti i giorni – l'unico metallo che ha una caratteristica distintiva unica. Questo perché il materiale attivo è in grado di essere magnetizzato dal campo magnetico. E la cessazione dell'ultimo ferro, era appena stato formato le proprietà magnetiche di cui, per lungo tempo è rimasto un magnete stesso. Questo fenomeno può essere spiegato dal fatto che la struttura del metallo è presente una pluralità di elettroni liberi, che sono in grado di muoversi.
In termini di chimica
Questo elemento si applica ai metalli attività media. Tuttavia, ferro chimica le proprietà sono tipiche per tutti gli altri metalli (diversi da quelli che si trovano a destra dell'idrogeno nella serie elettrochimica). E 'in grado di rispondere a molte classi di sostanze.
Cominciamo con il semplice
Ferrum reagito con kilorodom, azoto, alogeno (iodio, bromo, cloro, fluoro), fosforo, carbonio. La prima cosa da considerare – la reazione con oxygenic. Durante la masterizzazione Ferrum si formano i suoi ossidi. A seconda delle condizioni di reazione e le proporzioni tra le due parti, possono essere variate. Come esempio di tali interazioni può comportare la seguente equazione di reazione: 2Fe + O 2 = 2FeO; 4Fe + 3O 2 = 2Fe 2 O 3; 3Fe + 2O 2 = Fe 3 O 4. E proprietà di ossido di ferro (sia fisica che chimica) può essere variata, a seconda della sua varietà. Tali reazioni avvengono a temperature elevate.

Avanti – interazione con l'azoto. Può anche verificarsi solo a condizione di riscaldamento. Se prendiamo sei moli di ferro per mole di azoto ottenere due moli di nitruro di ferro. L'equazione di reazione è il seguente: 6Fe + N 2 = 2Fe 3 N.
Per reazione con fosforo è formato fosfuro. Per la reazione, sono tali componenti necessari: tre Ferrum moli – per mole di fosforo, è formato come un risultato di uno fosfuro mole. L'equazione può essere scritta come segue: 3Fe + P = Fe 3 P.
Inoltre, l'interazione può anche essere isolato tra sostanze reazioni di zolfo elementare. Così è possibile avere solfuro. Il principio su cui il processo di formazione della sostanza, simile a quelle sopra descritte. Vale a dire, v'è una reazione di addizione. Per tutte le interazioni chimiche di questo genere richiedono condizioni particolari, soprattutto in alta temperatura, almeno – catalizzatori.
È anche comune nella reazione chimica tra ferro e alogeni. Questa clorazione, bromurazione, iodurazione, fluorurazione. Come il nome stesso reazioni, un processo di adesione Ferrum atomi atomi di cloro / bromo / iodio / fluoro per formare cloruro / bromuro / ioduro / fluoruro rispettivamente. Questi materiali sono ampiamente utilizzati in una varietà di industrie. Inoltre, Ferrum grado di connettersi con il silicio ad alte temperature. A causa del fatto che le proprietà chimiche del ferro sono molteplici, è spesso utilizzato nell'industria chimica.
Ferrum e sostanze complesse
Da sostanze semplici passano alle molecole delle quali sono costituiti da due o più elementi chimici diversi. La prima cosa da menzionare – reazione Ferrum con l'acqua. Ci sono mostrate le proprietà di base di ferro. Quando l'acqua riscaldata insieme con ferro formata ossido basico (viene chiamato così perché forma un idrossido, in altre parole quando interagisce con la stessa acqua – base). Quindi, se prendiamo una mole di entrambi i componenti sono formate sostanze come l'anidride ferrum e gas idrogeno con un odore pungente – come in proporzioni molari di uno a uno. L'equazione di queste reazioni può essere scritto come segue: Fe + H 2 O = FeO + H 2. A seconda delle proporzioni in cui per miscelare i due componenti, si può ottenere una triossido di- o ferro. Entrambi questi agenti sono molto comuni nel settore chimico, e utilizzato anche in molti altri settori.
Con acidi e sali
Poiché Ferrum è lasciato dell'idrogeno nella serie elettrochimica di attività metalli, esso spososoben spostare elemento attivo di composti. Un esempio di questo è la reazione di sostituzione che può essere osservata quando si aggiungono ferro all'acido. Ad esempio, se miscelati in proporzioni uguali molari di ferro e acido solfato (alias solforico) concentrazione media, come risultato si ottiene ferro (II) solfato e idrogeno in proporzioni molari uguali. L'equazione di una tale reazione sarebbe simile a questa: Fe + H 2 SO 4 = FeSO 4 + H 2.
Durante l'interazione con i sali di ferro manifestato riducenti. Cioè, utilizzando può essere distinto da sali di metalli meno attivi. Ad esempio, se prendiamo una mole di solfato di rame e lo stesso Ferrum, possiamo ottenere solfato di ferro (II) e rame puro in proporzioni molari uguali.
Il valore per l'organismo
Uno dei più comuni nella crosta degli elementi chimici – ferro. Proprietà della materia che hanno già preso in considerazione, e ora veniamo ad esso da un punto di vista biologico. Ferrum ha una funzione molto importante a livello cellulare che a livello di tutto l'organismo. In primo luogo il ferro è la base di una proteina come l'emoglobina è. È necessario per il trasporto di ossigeno dal sangue dai polmoni a tutti i tessuti, organi, ad ogni cellula del corpo, specialmente ai neuroni cerebrali. Pertanto, le proprietà benefiche di ferro non può essere sottovalutata.

Inoltre colpisce kroveobrazovanie, Ferrum è anche importante per il normale funzionamento della ghiandola tiroidea (richiede non solo l'iodio, come alcuni credono). Inoltre, il ferro è coinvolto nel metabolismo intracellulare, regola il sistema immunitario. Più particolarmente ferrum in grande quantità si trova nelle cellule epatiche, in quanto contribuisce a neutralizzare le sostanze nocive. Egli è anche uno dei componenti principali di molti tipi di enzimi nel nostro corpo. La dieta umana quotidiana dovrebbe contenere da dieci a venti milligrammi di oligoelemento.
Gli alimenti ricchi di ferro
Tale sacco. Mangiano sia di origine vegetale e animale. In primo luogo – questo è cereali, legumi, cereali (in particolare grano saraceno), mele, funghi (bianco), frutta secca, bacche di rosa canina, pere, pesche, avocado, zucca, mandorle, fichi, pomodori, broccoli, cavoli, mirtilli, more, sedano, ecc . In secondo luogo – fegato, carne. Uso di un prodotto ad alto contenuto di ferro è particolarmente importante durante la gravidanza, come il corpo del feto formato richiede una grande quantità di micronutrienti per la crescita e lo sviluppo.
I segni di una carenza di ferro nel corpo
I sintomi di troppo piccola quantità di Ferrum entrare nel corpo sono la stanchezza, le mani ed i piedi di congelamento costante, la depressione, i capelli e le unghie fragili, riduzione di attività intellettuale, disturbi digestivi, basso rendimento, malfunzionamento della tiroide. Se notate alcuni di questi sintomi, è necessario aumentare il numero di prodotti contenenti ferro nella vostra dieta o per comprare vitamine o integratori contenenti Ferrum. Inoltre, assicurarsi di consultare il proprio medico se uno qualsiasi di questi sintomi si sente troppo male. 
Utilizzando Industria Ferrum
Applicazione e proprietà di ferro sono strettamente correlati. Grazie alla sua ferromagnetico, che viene utilizzato per la produzione di magneti – sia più debole per uso domestico (magneti souvenir sulla frigorifero, ecc …) e più potente – per scopi industriali. A causa del fatto che il metallo considerato ha ad alta resistenza e durezza, con la sua antichità utilizzato per le armi, armature e altri strumenti militari e nazionali. Tra l'altro, in Egitto è stato conosciuto ferro meteorico con proprietà superiori a quelle di un metallo convenzionale. Anche un ferro speciale è stato utilizzato nella Roma antica. Da essa ha prodotto un'arma d'elite. Scudo o una spada in metallo meteoriche, potrebbe avere solo un uomo molto ricco e distinto.

Generalmente, il metallo, che consideriamo in questo articolo, è il più versatile di tutte le sostanze impiegate dal gruppo. Prima di tutto, ha fatto di acciaio e ghisa, che vengono utilizzati per la produzione di vari prodotti necessari nell'industria e nella vita quotidiana.
Ghisa chiamato ferro e lega di carbonio, in cui la seconda presente dal 1.7 a 4.5 per cento. Se il secondo è inferiore al 1,7 per cento, allora questo tipo di lega nota come l'acciaio. Se carbonio è presente nella composizione di circa 0,02 per cento, allora è un ferro commerciale ordinario. La presenza di carbonio nella lega necessaria per conferire maggiore resistenza, stabilità termica, resistenza alla ruggine.
Inoltre, in acciaio può contenere molti altri elementi come impurità. Questo manganese e fosforo, e silicio. Anche in questo tipo di lega per impartire alcune qualità possono essere aggiunti cromo, nichel, molibdeno, tungsteno, e molti altri elementi chimici. Tipi di acciaio, in cui una grande quantità di silice presente (circa quattro per cento), usato come trasformatore. Quelli nella composizione di cui molte manganese (fino a dodici o quattordici per cento) trova applicazione nella fabbricazione di parti di ferrovie, mulini, smerigliatrici e altri strumenti, parti della quale sono soggetti a rapida abrasione.
Molibdeno viene introdotto nella composizione della lega, per renderlo più termicamente stabile – come l'acciaio utilizzato nello strumento. Inoltre, per ottenere tutte le noto e comunemente usato in famiglie sotto forma di coltelli e altri attrezzi domestici acciai inossidabili devono essere aggiunti in lega di cromo, nichel e titanio. E per ottenere resistente agli urti, ad alta resistenza, duttilità, è sufficiente aggiungere vanadio. Quando si entra nel niobio può raggiungere una elevata resistenza alla corrosione e sostanze chimicamente aggressivi.
magnetite minerale, che è stato menzionato in precedenza in questo articolo, è necessario per la produzione di hard disk, schede di memoria e altri dispositivi di questo tipo. A causa delle proprietà magnetiche di ferro può essere trovato nel dispositivo di trasformatori, motori, e altri prodotti elettronici. Inoltre, ferrum può aggiungere altre leghe metalliche per conferire una maggiore resistenza e stabilità meccanica. Solfato questo elemento è usato in orticoltura per controllare parassiti (insieme con solfato di rame).  cloruri di ferro sono indispensabili nella depurazione delle acque. Inoltre, la polvere di magnetite è utilizzata in stampanti in bianco e nero. Il metodo di applicazione principale del pirite – ne derivano acido solforico. Questo processo avviene in laboratorio in tre fasi. Nel primo passo pirite Ferrum bruciato invia ossido ferrico e biossido di zolfo. Il secondo passo è la trasformazione di biossido di zolfo nella sua triossido, con la partecipazione di ossigeno. E la fase finale del materiale risultante viene fatto passare attraverso il vapore acqueo in presenza di catalizzatori, e quindi dare acido solforico.
cloruri di ferro sono indispensabili nella depurazione delle acque. Inoltre, la polvere di magnetite è utilizzata in stampanti in bianco e nero. Il metodo di applicazione principale del pirite – ne derivano acido solforico. Questo processo avviene in laboratorio in tre fasi. Nel primo passo pirite Ferrum bruciato invia ossido ferrico e biossido di zolfo. Il secondo passo è la trasformazione di biossido di zolfo nella sua triossido, con la partecipazione di ossigeno. E la fase finale del materiale risultante viene fatto passare attraverso il vapore acqueo in presenza di catalizzatori, e quindi dare acido solforico.
ottenere ferro
Fondamentalmente metallo attivo viene estratto dai suoi due principali minerali: magnetite ed ematite. Farlo con una riduzione del ferro da suoi composti di carbonio sotto forma di coke. Questo viene fatto in un altoforno, in cui la temperatura raggiunge i duemila gradi centigradi. Inoltre, v'è un modo per ripristinare Ferrum idrogeno. A tale scopo la presenza eventualmente di un altoforno. Per implementare questo metodo richiede una particolare argilla, viene miscelato con il minerale frantumato e trattato con idrogeno in forno a tino.
conclusione
Le proprietà e le applicazioni di ferro varia. Questo è forse il più importante nella nostra vita di metallo. Diventando noto per l'uomo, ha preso il posto di bronzo, che a quel tempo era il principale materiale per la fabbricazione di utensili e armi. Acciaio e ferro in molti modi superiori alla lega di rame e stagno in termini di proprietà fisiche, resistenza alle sollecitazioni meccaniche.
Inoltre, il ferro sul nostro pianeta è più comune di quanto molti altri metalli. frazione di massa nella crosta terrestre è quasi il cinque per cento. È il quarto elemento chimico più abbondante in natura. Inoltre, questo elemento chimico è molto importante per il normale funzionamento del corpo di animali e piante, soprattutto perché si basa sulla emoglobina costruito. Il ferro è un oligoelemento essenziale, il cui uso è importante per la salute e il normale funzionamento degli organi. Oltre a quanto sopra, è l'unico metallo che ha proprietà magnetiche uniche. Senza Ferrum è impossibile immaginare la nostra vita.