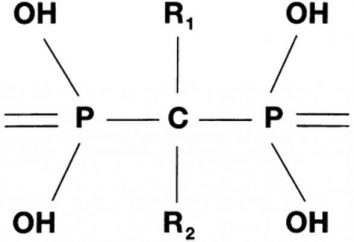
La reazione di CaCl2, H2SO4
Uno degli ostacoli nelle prime fasi di studio le leggi chimiche e le basi è quello di scrivere le reazioni chimiche. Pertanto, le domande circa l'interazione di CaCl2, H2SO4 non trovato periodicamente e sistematicamente. Esaminiamo le principali momenti "problema".
equazione molecolare Record
Interazione tra cloruro di calcio (sale) e acido solforico scorre attraverso il meccanismo di scambio.
 Caratteristiche di questa reazione sono:
Caratteristiche di questa reazione sono:
- due connessioni in entrata (materiale grezzo);
- due connessioni in uscita (prodotto);
- completa mancanza di sostanze semplici.
Scambiando tra loro gruppi reattivi, i reagenti sono modificate, e l'equazione assume la forma:
CaCl2 + H2SO4 = CaSO4 + 2HCl.
Come si vede, due sostanza complessa, ioni Cambiare forma molto diverse mescole: un nuovo sale (CaSO4) e acido cloridrico (HCl).
Per scorrere fino alla fine
Rispondere a questa domanda può essere semplicemente scrivendo a CaCl2, equazione di reazione H2SO4 in forma molecolare. Il tipo di prodotti e tutti dipendono. Fino alla fine del processo è nel caso di istruzione:
- materiale solubile (fanghi);
- composto volatile (gas);
- reagente malodissotsiiruschego (acqua, elettroliti deboli).
In considerazione per il caso di CaCl2, H2SO4 là tra prodotti di reazione di solfato di calcio – composto poco solubile precipita in base alla tabella.
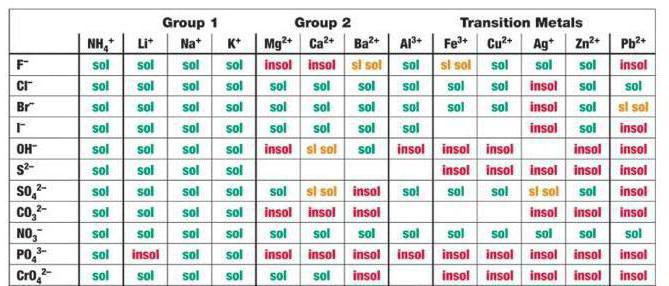
Di conseguenza, il processo di scambio si terrà fino alla fine.
forma ionica sintetizzati tra registrazione CaCl2, H2SO4
Scrivendo tutti i composti solubili in ioni e riducendo ricorrenti gruppi reattivi, si ottengono due equazioni sconosciuti:
- completa registrazione forma ionica tra CaCl2, H2SO4
Ca2 + + 2 cl – + 2h + + in modo 4 2- = Caso 4 + 2h + + 2 cl –
- una forma abbreviata dell'equazione
Ca 2 + + SO 4 2- = CaSO 4.
Va ricordato che solo gli ioni dipinte sali solubili, acidi, basi (questo è facilmente desumibile da apposite tabelle). Debole elettroliti tipo carbonico o acido acetico è sempre scritto in forma molecolare.
Ora si sa come l'interazione tra cloruro di calcio (sale), e acido solforico.