La formula generale per alcheni. Proprietà e caratterizzazione di alcheni
Le più semplici composti organici comprendono idrocarburi saturi e insaturi. Questi includono sostanze alcani classe, alchini, alcheni. 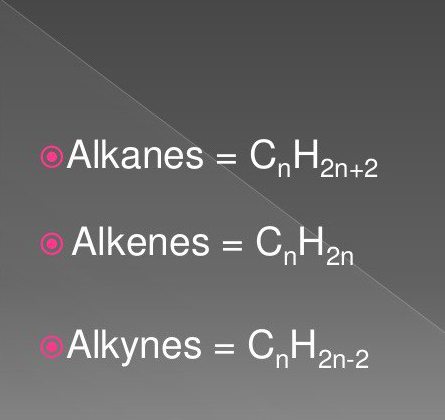
La formula dei quali comprendono idrogeno e atomi di carbonio in una sequenza e quantità specifica. Essi si trovano spesso in natura.
Determinazione di alcheni
Altro il loro nome – o idrocarburi olefine etilene. È così chiamata classe di composti attivi in 18 ° secolo, quando si aprono liquido oleoso – cloruro di etilene.
Da alcheni sono sostanze composte da elementi carbonio e idrogeno. Appartengono agli idrocarburi aciclici. Queste molecole sono presenti solo doppio (insaturo) legame che collega i due atomi di carbonio tra loro.
alcheni formula
Ogni classe di composti ha una denominazione chimica. I simboli sono elementi del sistema periodico indicato la composizione e la struttura della connessione di ciascuna sostanza. 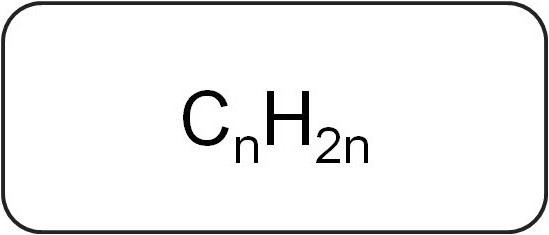
La formula generale dei alcheni indicati come segue: C n H 2n, dove il numero n è maggiore o uguale a 2. Se decifrazione si può notare che ciascun atomo di carbonio ha due atomi di idrogeno.
alcheni formula molecolare della serie omologa rappresentato dalle seguenti strutture: C 2 H 4, C 3 H 6, C 4 H 8, C 5 H 10 C 6 H 12, C 7 H 14, C 8 H 16 C 9 H 18, C 10 H 20. Si può notare che ciascun idrocarburo successiva contiene uno più carbonio in idrogeno 2 e più.
C'è una posizione simbolo grafico e l'ordine di composti chimici tra atomi nella molecola, che mostra la formula di struttura di alcheni. Con l'aiuto di valenza indicato dal carbonio e idrogeno.
formula strutturale alcheni può visualizzare in forma espansa, quando presenti, tutti gli elementi chimici e connessioni. Un'espressione più concisa non è mostrata composto olefine carbonio e idrogeno mediante valenza.
Formula designato scheletrico la struttura più semplice. linea tratteggiata rappresenta il fondamento della molecola in cui gli atomi di carbonio vengono rappresentati con i suoi piani e finisce, e collegamenti punto idrogeno.
Come per formare il nome di olefine
Basata sulla nomenclatura sistematica, formula e nomi di alcheni da alcani costituire la struttura riguardante gli idrocarburi saturi. Per fare questo nel nome dell'ultimo suffisso -Un sostituito dal -ilen o -en. Un esempio è la formazione di butano-butilene e pentene da pentano.
Per indicare la posizione relativa alla doppia connessione di atomi di carbonio indicati in numeri arabi alla fine del nome.
Al centro dei nomi di alcheni è la designazione dell'idrocarburo con la catena più lunga in cui il doppio legame è presente. Durante l'avviamento numerazione della catena è tipicamente selezionato estremità che è più vicino al composto insaturo, atomi di carbonio.
Se la formula di struttura di alcheni ha rami che indicano il nome radicali e numero, e per dare loro cifre posto corrispondente nella catena di carbonio. Seguito dal nome dell'idrocarburo. Dopo che i numeri sono di solito mettere un trattino.
Ci propaggini radicali insaturi. I loro nomi possono essere banali o formato dalle regole della nomenclatura sistematica.
Ad esempio, NSC = CH- cui etenile o vinile.
isomeri
alcheni formula molecolare non possono indicare l'isomeria. Tuttavia, per questa classe di sostanze, ad eccezione del etilene molecola variazione spaziale intrinseca. 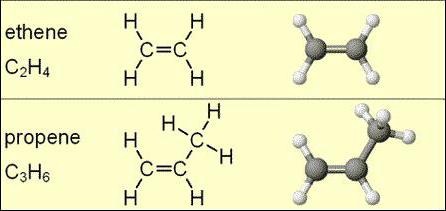
Isomeri idrocarburi etileniche possono essere sullo scheletro di carbonio, di insaturi interclasse posizione comunicazione o spaziale.
La formula generale dei alcheni determina la quantità di carbonio ed idrogeno atomi nella catena, ma non mostra la presenza e la posizione di un doppio legame in esso. Un esempio è il ciclopropano come un cross-classe Isomero C 3 H 6 (propilene). Altri tipi di isomeria, sono esposti a C 4 H 8 o butene.
Varie stato della comunicazione insaturo si verifica nel butene-1 o butene-2, nel primo caso, una doppia connessione è vicino al primo atomo di carbonio, e nel secondo – nel mezzo della catena. Isomeri di scheletro di carbonio possono essere considerati per esempio metilpropene (CH 3 -C (CH 3) = CH 2) e isobutilene ((CH3) 2C = CH 2).
variazione spaziale intrinseca posizione butene-2 e cis-trans. Nel primo caso i gruppi laterali si trovano sopra e sotto la catena di carbonio principale con un doppio legame nel secondo sostituenti isomeriche sono sullo stesso lato.
Caratteristiche di olefine
La formula generale per alcheni determina la condizione fisica di tutti i membri di questa classe. Iniziando e terminando con etilene butilene (C 2 a C 4), sostanze esistono in forma gassosa. Così etene incolore ha odore dolciastro, bassa solubilità in acqua, peso molecolare inferiore a quella dell'aria.
In forma liquida, idrocarburi presentato periodo omologo da C 5 -C 17. Cominciando con l'alchene avente nella catena principale di 18 atomi di carbonio, un transizione dello stato fisico in forma solida.
Tutti olefine rango scarsa solubilità in mezzi acquosi, ma buono nella natura organica del solvente quale benzene o benzina. Il loro peso molecolare è inferiore a quella dell'acqua. Aumentando i cavi catene di carbonio ad un aumento di temperatura da caratteristiche di fusione e di ebollizione di questi composti.
proprietà olefine
alcheni formula strutturale dimostra la presenza di doppio legame nello scheletro e σ- di π- collegano due atomi di carbonio. Questa struttura della molecola determina le proprietà chimiche. Comunicazione-π è considerato non molto forte, il che rende possibile distruggerlo con la formazione di due nuovi legami-σ, che si ottengono come risultato di aderire ad una coppia di atomi. Gli idrocarburi insaturi sono donatori di elettroni. Partecipano ai processi di tipo connection elettrofila. 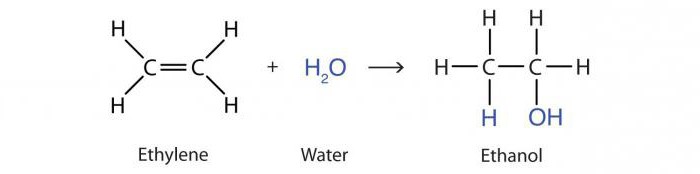
Un'importante proprietà chimica di alcheni è un processo di alogenazione con il rilascio di composti tali sostanze digalogenoproizvodnym. atomi di alogeno possono essere collegati al composto da doppie carboni. Un esempio è la bromurazione di propilene per formare il 1,2-dibromopropano:
H 2 C = CH-CH 3 + Br 2 → BrCH 2 -CHBr-CH 3.
Questo colori processo di neutralizzazione in acqua di bromo alcheni considerati dimostrazione qualitativa della presenza di doppio legame.
importanti reazioni olifinov riferisce idrogenazione con l'aggiunta di molecole di idrogeno sotto l'azione di metalli catalizzatore quale platino, palladio o nickel. Ciò si traduce in idrocarburi con un legame saturo. alcani Formula, alcheni sono riportati di seguito nella idrogenazione di butene:
CH 3 -CH 2 -CH = CH 2 + H 2 → CH 3 Ni -CH 2 -CH 2 -CH 3.
Il processo di adesione molecole alogenuri dette olefine
gidrogalogenirovaniem passando dalla regola, aperto Markovnikov. Un esempio è la hydrobromination di propilene per formare 2-bromopropano. È collegato con il doppio legame idrogeno-carbonio, che è considerato il più idrogenato:
CH 3 -CH = CH 2 + HBr → CH 3 -BrCH-CH 3.
reazione di addizione con acidi acqua alcheni è noto come idratazione. Il risultato è una molecola di alcol 2-propanolo :
CH 3 -HC = CH 2 + H 2 O → CH 3 -OHCH-CH 3.
Quando esposti agli alcheni solforico processo di solfonazione acido verifica:
CH 3 CH 2 = -HC + HO-OSO-OH → CH 3 -CH 3 CH-OSO 2 -OH.
La reazione procede con la formazione di esteri di acidi, ad esempio acido izopropilsernoy.
Alcheni sensibili all'ossidazione durante la loro combustione sotto l'azione di ossigeno per formare acqua e anidride carbonica:
2CH 3 -HC = CH 2 + 2 9O → 6CO 2 + 6H 2 O.
La reazione dei composti olefinici e un permanganato di potassio diluita in soluzione dà luogo ad una struttura glicoli o alcoli bivalenti. Questa reazione è anche ossidante per formare glicole etilenico e soluzione sbianca:
3H 2 C = CH 2 + 4H 2 O + 2KMnO 4 → 3OHCH-CHOH + 2MnO 2 + 2KOH.
molecola di alchene può essere coinvolto nella polimerizzazione con un meccanismo radicale o cationica-anionica libera. Nel primo caso, sotto l'influenza di perossidi ottenuti tipo polietilene polimero.
Secondo il secondo meccanismo catalizzatori cationici sono gli agenti acidi e anionici sono polimeri metallorganico con allocazione stereoselettiva.
Qual è alcani
Essi sono chiamati paraffine o limitano idrocarburi aciclici. Hanno una struttura lineare o ramificata, che contiene solo legami singoli saturi. Tutti i membri della serie omologa di questa classe hanno formula generale C n H 2n + 2. 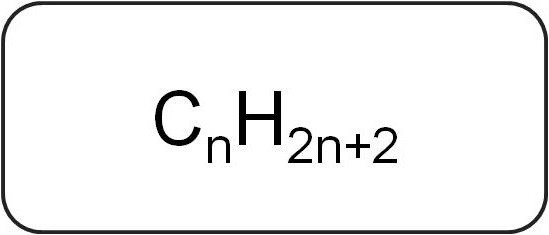
Nella loro struttura contiene soltanto atomi di carbonio e di idrogeno. La formula generale dei notazione idrocarburi saturi alchene formata.
I nomi di alcani e le loro caratteristiche
Il rappresentante più semplice di questa classe è il metano. Seguita da sostanze quali etano, propano e butano. La base del loro nome è la radice della cifra in lingua greca, a cui si aggiunge il suffisso -an. nomi alcani sono elencati nella nomenclatura IUPAC.
La formula generale per alcheni, alchini, alcani comprende solo due specie di atomi. Questi includono elementi carbonio e idrogeno. Il numero di atomi di carbonio in tutte le tre classi di corrispondenze, contrasto viene osservata solo nel numero di idrogeno che può essere scisso o aderire. idrocarburi saturi ottenuti composti insaturi. I rappresentanti delle paraffine contenute nella molecola è 2 atomi di idrogeno più l'olefina, che conferma una formula generale di alcani, alcheni. Struttura alcheni è considerata dovuta alla presenza di doppio legame insaturo.
Se si confronta il numero di idrogeno e carbonio atomi nel alcano, il valore massimo sarà confrontata con altre classi di idrocarburi.
Poiché metano e termina butano (C 1 a C 4), sostanze esistono in forma gassosa.
In forma liquida, idrocarburi presentato periodo omologo da C 5 -C 16. Poiché alcano avente nella catena principale di 17 atomi di carbonio, un transizione dello stato fisico in forma solida.
Essi sono caratterizzati da isomeria dello scheletro di carbonio e modifiche ottiche della molecola. 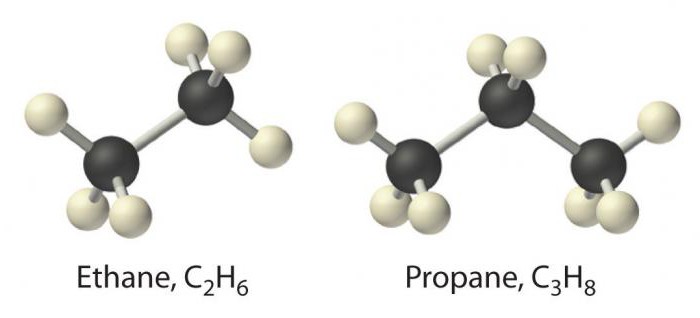
Le valenze paraffine carbonio sono considerati carboni adiacenti completamente occupate o idrogeno per formare una connessione σ-type. Dal punto di vista chimico, questo provoca loro proprietà più deboli, motivo per cui alcani sono chiamati limite o idrocarburi saturi privi di affinità.
Entrano in reazioni di sostituzione relativi a alogenazione da un sulfochlorination tipo nitrazione radicale o molecola.
Paraffine subiscono un processo di ossidazione, combustione o decomposizione a temperature elevate. Sotto gli acceleratori azione reazioni scissione avvengono un atomo di idrogeno o deidrogenazione di alcani.
Qual è alchini
Sono anche chiamati idrocarburi acetilene, in cui è presente nel triplo legame carbonio catena. La struttura del alchino descritto dalla formula generale C n H 2 n-2. Si può notare che in contrasto alcani da idrocarburi acetilenici manca quattro atomi di idrogeno. Essi sostituiscono il triplo legame, formato da due collegamenti π-.
Questa struttura determina le proprietà chimiche di questa classe. La formula di struttura di alcheni e alchini dimostra insaturazione delle molecole e la presenza di doppio (H 2 C꞊CH 2) e collegamento tripla (HC≡CH).
Nome alchini e le loro caratteristiche
Il rappresentante più semplice è l'acetilene o HC≡CH. E 'indicato anche come etinile. Deriva dal nome del idrocarburico saturo, che ha rimosso il -una suffisso e aggiungere -in. Nei nomi di figura lunga alkyne indicare la posizione del triplo legame.
Conoscendo la struttura dell'idrocarburo saturi e insaturi, può essere determinato con lettera indica la formula generale per alchini: a) CnH2n; a) CnH2n + 2; c) CnH2n-2; g) CnH2n-6. La risposta corretta è la terza opzione.
Partendo da butano acetilene e termina (C 2 a C 4), sostanze sono gassoso in natura. 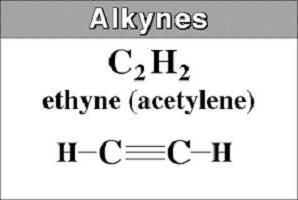
In idrocarburi in forma liquida sono omologhe periodo da C 5 -C 17. Partendo con alkyne aventi nella catena principale di 18 atomi di carbonio, un transizione dello stato fisico in forma solida.
Essi sono caratterizzati da isomeria dello scheletro di carbonio, sulla condizione della comunicazione triple e interclassista modifica molecola.
Da caratteristiche chimiche simili idrocarburi acetilenici alcheni.
Se il triplo legame alchino terminale, operano per formare un acido sali funzione alkinidov, ad esempio, NaC≡CNa. La presenza dei due ¸ legami rende la molecola un forte sodio nucleofilo atsetiledina entrare in reazioni di sostituzione.
Acetilene viene clorurato in presenza di cloruro di rame per ottenere dicloroacetile, condensazione sotto l'azione di un rilascio aloalchinile molecole diacetylenic.
Alchini partecipano a reazioni di addizione elettrofila, il principio che è alla base alogenazione gidrogalogenirovaniya, idratazione e carbonilazione. Tuttavia, tali processi sono più debole di quella di alcheni con un doppio legame.
Per idrocarburi acetilenici possono nucleofila reazione di addizione della molecola tipo alcool, un'ammina primaria o solfuro.