Molecola: un peso molecola. Le dimensioni e la massa delle molecole
La composizione dei materiali complessi, anche se sono formati da minuscole particelle – atomi, molecole, ioni. La struttura molecolare ha molti liquidi e gas, e anche alcuni corpo solido. Atomi e ioni metallici, comprendono molti sali. Tutte le particelle hanno massa, anche la molecola più piccola. Messa della molecola, se l'esprimiamo nei chili, riceve un valore molto piccolo. Per esempio, m (H 2 O) = 30 • 10 -27 kg. Tali caratteristiche importanti di una sostanza come il peso e le dimensioni delle microparticelle, è stato a lungo studiati fisici e chimici. Le fondamenta sono state gettate nelle opere di Mikhail Lomonosov e Dzhona Daltona. Considerare come cambiato dal punto di vista sulla microcosmo.
Presentazione Università di "corpuscoli"
L'assunzione di discreta struttura della materia espressa da studiosi dell'antica Grecia. Poi è stato dato il nome di "atomo" la più piccola particella indivisibile di organi, "mattoni" dell'universo. Il grande studioso russo M. V. Lomonosov ha scritto circa le proprietà fisico trascurabile e indivisibile significa struttura particella di materia – corpuscolo. Più tardi, negli scritti di altri studiosi, è stata chiamata "molecola".
molecola di massa e le sue dimensioni sono determinate dalle proprietà dei suoi atomi costituenti. Per molto tempo gli scienziati non sono stati in grado di guardare più in profondità nel microcosmo che ostacolato lo sviluppo della chimica e della fisica. Lomonosov ripetutamente esortato i colleghi di apprendere e nel loro lavoro sulla base di dati quantitativi accurati – "misura e il peso" di un Attraverso il lavoro di chimico russo e fisico posto le basi della dottrina della struttura della materia, che sono diventati parte integrante coerente teoria atomico-molecolare.

Atomi e molecole – "mattoni dell'universo"
Anche microscopicamente piccoli oggetti difficili da trovare, hanno proprietà diverse. Particelle come atomi, formata dal nucleo e gli strati elettronici differiscono nel numero di cariche positive e negative Raggio peso. esistono atomi e molecole nella composizione di sostanze, non isolatamente, sono attratti forza diversa. effetto più evidente delle forze di attrazione nei solidi, più debole – in liquidi, appena sentito nelle sostanze gassose.
Le reazioni chimiche non sono accompagnati da atomi di distruzione. Il più delle volte, v'è un raggruppamento di loro, c'è un'altra molecola. molecola di massa dipende da ciò che gli atomi si forma. Ma con tutti i cambiamenti negli atomi sono chimicamente indivisibile. Ma possono diventare parte di molecole diverse. Gli atomi mantengono le proprietà dell'elemento a cui il. Molecola prima di decadere in atomi mantiene tutti gli attributi della sostanza.
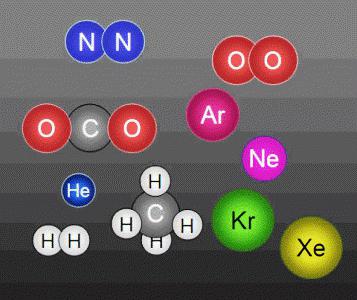
Struttura microparticelle di corpi – molecola. la massa della molecola
Per misurare i macrobodies di massa vengono utilizzati dispositivi, la più antica delle quali – scale. Il risultato della misurazione viene convenientemente preparato in chilogrammi, come unità di base di grandezze fisiche del sistema internazionale (SI). Per determinare la massa molecolare in chilogrammi, è necessario stabilire i loro pesi atomici in base al numero di particelle. Per comodità, una speciale unità di massa è stata introdotta – nucleare. Si può scrivere in forma di lettera abbreviazioni (amu). Questa unità corrisponde ad un dodicesimo della massa del nuclide di carbonio 12 C.
Se esprimiamo il valore trovato in unità standard, otteniamo 1,66 • 10 -27 kg. Tali piccole indicatori per gli organismi di massa operano principalmente fisica. L'articolo è una tabella da cui si può imparare quali sono le masse degli atomi di alcuni elementi chimici. Per scoprire quale è la massa di una molecola di idrogeno in chilogrammi, moltiplicare per due mostrate nella tabella massa atomica dell'elemento chimico. Il risultato è un valore di peso molecole costituite da due atomi.
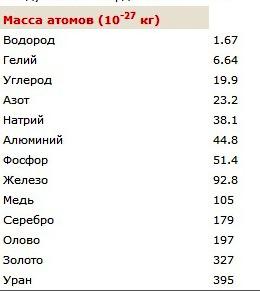
massa molecolare relativa
È difficile operare nel calcolo di quantità molto piccole, è scomodo, porta a tempo, soggetto a errori. Per quanto riguarda il peso delle microparticelle, quindi il rilascio della situazione difficile è stato l'uso di valori relativi. Familiar ai chimici termine è costituito da due parole – "massa atomica", il suo simbolo – Ar. concetto identico è stato introdotto al peso molecolare (uguale alla massa della molecola). La formula relativa delle due grandezze: Mr = m (target) / 1/12 m (12 C).
Spesso si può sentire quello che dicono "peso molecolare". Questo termine obsoleto usato anche rispetto al peso molecolare, ma meno frequentemente. Il fatto che il peso – è una grandezza fisica differente – la cui potenza dipende dalle coordinate geografiche del corpo. Al contrario, la massa è una caratteristica costante delle particelle che partecipano a processi chimici, e sono spostati a velocità normale.

Come determinare il peso molecolare
La definizione esatta del peso molecola viene effettuata dallo strumento – spettrometro di massa. Per risolvere i problemi, è possibile utilizzare le informazioni della tavola periodica. Ad esempio, la massa di una molecola di ossigeno è 2 • 16 = 32. Eseguiamo calcoli semplici e trovare il valore di sig (H 2 O) – peso molecolare relativo di acqua. Da tavola periodica definito che la massa di ossigeno – 16, l'idrogeno – 1. Draw semplice calcolo: M r (H 2 O) = 1 + 2 • 16 = 18, dove M r – peso molecolare, H 2 O – molecola d'acqua, H – idrogeno elemento simbolo O – chimica di ossigeno segno.
masse di isotopi
Elementi chimici in natura e tecnologia esistono come diverse specie di atomi – isotopi. Ciascuno di essi ha un peso unitario, il suo valore non può essere un valore frazionario. Tuttavia, il peso atomico dell'elemento chimico spesso è un numero con molteplici segni dopo la virgola. Quando i calcoli tengono conto della prevalenza di ciascuna specie nella crosta terrestre. Pertanto, la massa degli atomi della tavola periodica non sono necessariamente interi. L'utilizzo di questi valori per i calcoli, si ottiene la massa delle molecole, che non sono anche interi. In alcuni casi, può essere un valore di arrotondamento.
Il peso molecolare di struttura non molecolare della materia
La maggior parte composti inorganici non sono struttura molecolare. Metalli sono composti da atomi, ioni ed elettroni liberi, sali – di cationi e anioni. Per le sostanze strutture peso molecolare non contate anche molecole condizionali di formula lordo, riflettendo la struttura più semplice. Troviamo il valore signor per la struttura sostanze ioniche – sale la cui formula NaCl. M r = 23 + 35,5 = 55,5. Per alcuni tipi di calcoli richiesti massa molecolare dell'aria – miscela di gas. Considerando la percentuale delle diverse sostanze nell'atmosfera, molecolare massa dell'aria è 29.
Le dimensioni e la massa delle molecole
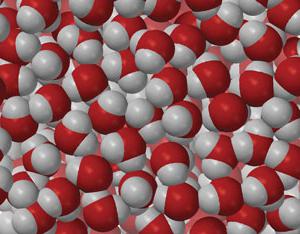
microscopio elettronico di grandi molecole possono prendere in considerazione i singoli atomi, ma sono così piccole che un microscopio ordinario non può essere visto. granulometria lineare di qualsiasi sostanza come il peso, – una caratteristica costante. Il diametro della molecola dipende raggi dei suoi atomi costituenti, la loro reciproca attrazione. Le dimensioni delle particelle variano con il numero di protoni e livelli di energia. Atomo di idrogeno – la più piccola dimensione, il suo raggio è solo 0,5 • 10 -8 atomo cm uranio è tre volte più atomi di idrogeno .. Questi "giganti" del microcosmo – le molecole delle sostanze organiche. Così, uno della dimensione lineare della particella proteina è 44 • 10 -8 cm.
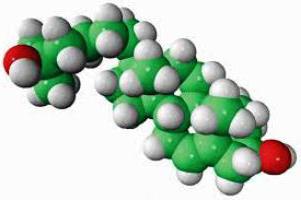
Per riassumere: la massa delle molecole – è la somma delle masse di atomi al loro interno. Il valore assoluto in chilogrammi può essere ottenuto moltiplicando il peso molecolare trovato nella Tavola Periodica, la quantità 1,66 • 10 -27 kg.
Le molecole sono trascurabili rispetto alle macro organismi. Ad esempio, in termini di dimensioni della molecola d'acqua H 2 O dà la mela come tante volte, quante volte questo frutto è più piccolo del nostro pianeta.