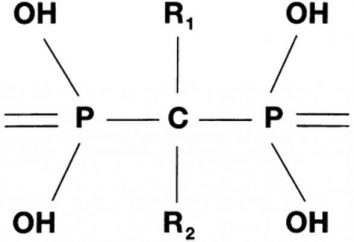
Chimica inorganica – che cosa è questo? chimica inorganica nel curriculum scolastico
Naturalmente chimica nelle scuole inizia nel grado 8 studiare i principi generali della scienza: descrivere i possibili tipi di legami tra gli atomi, tipi di reticolo cristallino ei meccanismi di reazione più comuni. Questo diventa la base per lo studio della sezione importante, ma più specifico – inorganici.

Che cos'è questo
Inorganica Chimica – la scienza che considera i principi della struttura, proprietà di base e reattività della tavola periodica degli elementi. Un ruolo importante è giocato nelle inorganici legge periodica, che regola la classificazione sistematica delle sostanze di cambiare il loro peso, numero e tipo.
Il corso comprende composti formati facendo reagire elementi di tabella (l'unica eccezione è la regione di idrocarburi, considerata nei capitoli organici). Compiti in chimica inorganica permettono di soddisfare le conoscenze teoriche nella pratica.

Science in prospettiva storica
Il nome "inorganico" apparso in accordo con l'idea che copre una parte della conoscenza chimica, che non è collegato con l'attività di organismi biologici.
Nel corso del tempo, è stato dimostrato che la maggior parte del mondo organico in grado di produrre e "non-vita" di un composto, e qualsiasi tipo di idrocarburi sintetizzati in laboratorio. Così, cianato di ammonio, che sale elementi di chimica scienziato Wohler tedesco potrebbe sintetizzare urea.
Per evitare confusione con la nomenclatura e classificazione dei tipi di ricerca del programma di due scienze di corsi scolastici e universitari dovrebbe essere per chimica generale comporta lo studio di inorganico come disciplina fondamentale. Nel mondo scientifico viene salvato sequenza analoga.
Classi sostanze inorganiche
Chimica tali mangimi fornisce un materiale in cui capitoli introduttivi considerano inorganico legge periodica elementi. Questa classificazione è un tipo speciale, che si basa sul presupposto che gli oneri nucleari atomiche hanno un impatto sulle proprietà delle sostanze e opzioni variare ciclicamente. Inizialmente tavolo costruito come un riflesso di elementi di massa atomica più grandi, ma presto una data sequenza è stata respinta a causa del suo fallimento nel aspetto in cui richiedono considerazione di questa materia, materia inorganica.
Chimica, oltre alla tavola periodica, suggerisce la presenza di un centinaio di forme, cluster e grafici che mostrano le proprietà di frequenza.
versione consolidata attualmente popolare del corrispettivo di concetti come classi di chimica inorganica. Le colonne degli elementi di tabella sono specificate in funzione delle proprietà fisico-chimiche, in linee – simili tra loro periodi.
sostanze semplici in sostanze inorganiche
Il segno nella tavola periodica e una semplice sostanza in uno stato libero – spesso due cose diverse. Nel primo caso si riflette solo un tipo specifico di atomi, nel secondo – il tipo di particelle del composto e la loro influenza reciproca in forme stabili.
legame chimico in sostanze semplici li fa dividere la famiglia. Così, due grandi gruppi di specie di atomi possono distinguere – metalli e non metalli. La prima famiglia comprende 96 membri da 118 studiati.

metalli
metallo tipo presuppone un collegamento tra le particelle dello stesso nome. Interazione basata su elettroni socializzazione reticolari, caratterizzato omnidirezionale e insaturi. Questo è il motivo per metalli sono buoni conduttori di calore, carica, ha una lucentezza metallica, malleabilità e duttilità.
Convenzionalmente, i metalli vengono lasciati nella tavola periodica durante linea retta dalla boro astato. Elementi che sono simili in luogo a questa linea, sono spesso natura di confine e presentano una dualità delle proprietà (per esempio, germanio).
Metalli forma più elementare del composto. Il grado di ossidazione di tali sostanze in genere non supera due. Sotto aumenti metallicità e diminuzioni del periodo. Ad esempio, francio radioattivo presenta una struttura di base di sodio e una famiglia alogeno hanno iodio comparire anche lucentezza metallica.
Diversa è la situazione in un periodo di – sottolivelli completati gas inerti, prima che sono sostanze con proprietà opposte. Nello spazio orizzontale della tavola periodica degli elementi esposti cambiamenti reattività da base per anfotero acido attraverso. Metalli – riducendo buona agenti (accettare elettroni nella formazione di legami).
Metalloidi
Questo tipo di atomi comprende le principali classi di chimica inorganica. Metalloidi occupano la parte destra della tavola periodica, tipicamente presentante proprietà acide. Gli elementi di dati più comunemente presenti in forma di composti tra loro (ad esempio, borati, solfati, acqua). Nello stato molecolare libera è noto l'esistenza di zolfo, ossigeno e azoto. Ci sono anche diversi non metallici gas biatomici – oltre al due di cui sopra, questi includono idrogeno, fluoro, bromo, cloro e iodio.

Sono le sostanze più abbondanti sulla terra – particolarmente comune silicio, idrogeno, ossigeno e carbonio. Iodio, selenio e arsenico distribuiti molto piccola (qui è possibile includere configurazioni radioattive e instabili, che si trovano nell'ultimo periodo della tavola).
Nei composti di elementi non metallici comportarsi prevalentemente come acidi. Sono potenti ossidanti dovuta alla possibilità di unione di elettroni supplementari per completare il livello.
sostanze complesse in sostanze inorganiche
Aggiunta di sostanze che sono rappresentati da un gruppo di atomi distinguere composti comprendenti diverse configurazioni. Tali sostanze possono essere binario (costituito da due particelle differenti), tre, quattro elementi e così via.
sostanze di due elementi
Di particolare importanza in connessione molecole binarity chimica allegate. Classi di composti inorganici sono considerati dalla prospettiva di collegamento formato tra gli atomi. Può essere ionico, metallico, covalente (polare o non polare) o misto. Tipicamente tali agenti mostrano chiaramente di base (per metallo stock), anfoteri (dual – particolarmente vero per l'alluminio) o acido (se v'è un elemento in stato di ossidazione +4 o superiore) qualità.
Tre soci elemento
Soggetti forniscono Inorganica Chimica considerazione e questo tipo di atomi di associazione. I composti costituiti da più di due gruppi di atomi (solitamente sui inorganica con i tipi tre pezzi) sono tipicamente formate con la partecipazione di componenti che differiscono significativamente l'uno dall'altro in parametri fisico-chimici.
Possibili tipi di comunicazione – covalente, ionico e misti. Tipicamente, tre elementi sostanza del comportamento simile a binario per il fatto che una delle forze interatomiche molto più forte altro: leggermente generato secondariamente e ha la capacità di dissociarsi in soluzione veloce.
Classi di chimica inorganica
La stragrande maggioranza studiata nei sostanze inorganiche corso può essere considerato per una semplice classificazione in base alla loro composizione e proprietà. Così, distinguere idrossidi, acidi, ossidi e sali. Considerazione del loro rapporto è meglio iniziare con un'introduzione al concetto di forme ossidate, che possono essere quasi qualsiasi sostanze inorganiche. La chimica di tali collegate discusso nei capitoli sugli ossidi.

ossidi
Ossido è un composto di qualsiasi elemento chimico con ossigeno in uno stato di ossidazione pari a -2 (come perossidi -1 rispettivamente). formazione del legame verifica a causa di impatto elettronico e riduzione degli stessi con O 2 (dove elemento più elettronegativo è ossigeno).
E può essere acido, e anfoteri, e le proprietà a seconda del secondo gruppo di atomi. Se questo metallo nell'ossido non superi +2 stato di ossidazione, se un non-metallo – da 4 e superiori. I campioni con i parametri del duplice natura raggiunti valore 3.
inorganici acido
composti acidi del mezzo di reazione è inferiore a 7 dal contenuto di idrogeno dei cationi che possono andare in soluzione e poi sostituito da uno ione metallico. Secondo la classificazione sono sostanze complesse. La maggior parte degli acidi possono essere preparate diluendo con acqua ossidi corrispondenti, per esempio, nella formazione di acido solforico dopo l'idratazione di SO 3.

Chimica inorganica di base
Le proprietà dei composti di questo tipo a causa della presenza del radicale ossidrile OH, che permette di reazione superiore a 7. Le basi alcalini solubili sono chiamati, sono i più potenti in questa classe di sostanze a causa della dissociazione completa (scomposizione in ioni nel liquido). Gruppo OH nella formazione di sali può essere sostituito con residui acidi.
Chimica inorganica – una duplice scienza che può descrivere la questione da una prospettiva diversa. In teoria di base protolytic considerati idrogeno accettori catione. Questo approccio estende il concetto di questa classe di sostanze, alcali chiamare qualsiasi sostanza che può accettare un protone.
sali
Questo tipo di composti è situato tra le basi e acidi, come prodotto della loro interazione. Così, come il catione serve tipicamente uno ione metallico (talvolta ammonio, fosfonio o hydronium) nonché sostanze anioniche – residuo di acido. Quando la formazione di sale viene sostituito da idrogeno con un'altra sostanza.
A seconda del rapporto di reagenti e forza rispetto all'altro trattare efficacemente diversi tipi di prodotti di reazione:
- sali basici vengono ottenuti se i gruppi ossidrilici non sono interamente sostituiti (tali sostanze mezzo di reazione alcalina);
- sali acidi si formano nel caso opposto – con la mancanza di base idrogeno parziale reattiva rimane nella connessione;
- le medie più noti e di facile comprensione sono (o normale) campione – sono il prodotto di reagenti di neutralizzazione completi per formare acqua e una sostanza con solo un catione metallico o un suo analogo e una parte acida.
Chimica inorganica – la scienza che consiste nel dividere ogni classe in frammenti, che sono considerati in momenti diversi: uno – prima di altri – più tardi. In uno studio approfondito di distinguere anche 4 tipi di sali:
- Duale contiene un singolo anione in presenza dei due cationi. Tipicamente tali materiali sono il risultato di fusione di due sali con lo stesso residuo acido, ma diversi metalli.
- fronte misto della precedente: è la base di un catione con due differenti anioni.
- Cristallini idrati – sale, in cui formula è l'acqua allo stato cristallino.
- Complessi – le sostanze in cui il catione, anione o entrambi sono rappresentati sotto forma di cluster con generatore. Tali sali possono essere preparati vantaggiosamente da elementi del sottogruppo B.

Come altre sostanze in un laboratorio su Inorganic Chemistry, che possono essere classificati come sali o idruri come conoscenza individuale capitoli si possono menzionare, nitruri, carburi e composti intermetallici (composti di metalli diversi, non legati).
risultati
Chimica inorganica – la scienza che è di interesse per ogni specialista in questo campo, a prescindere dalla loro interessi. Esso comprende il primo capitolo, ha studiato presso la scuola sul tema. Corso di Chimica Inorganica fornisce sistemazione di grandi volumi di informazioni secondo una classificazione chiara e semplice.